发病机制
发病机制
发病机制:
1.结节性多动脉炎的
血管损伤的机制目前也并不十分清楚。部分与
乙肝病毒感染相关的结节性多动脉炎,
乙肝病毒抗原诱导的免疫复合物能激活补体,诱导和活化中性粒细胞引起局部的血管炎症损伤。
(1)细胞因子在结节性多动脉炎的发病机制中起重要作用。结节性多动脉炎患者外周血清中α-干扰素、白细胞介素-2、α-肿瘤坏死因子、白细胞介素-1等的水平均明显升高。它们能诱导黏附分子(L
FA-1、ICAM-1和ELAM-1)的表达,从而使中性粒细胞易与血管内皮细胞接触,以及诱导血管内皮细胞的损伤。另外,结节性多动脉炎患者血清中常可检测到抗血管内皮细胞抗体。抗内皮细胞抗体可直接作用于血管内皮细胞表面,通过抗体依赖的细胞毒的作用介导血管内皮的损伤。
(2)免疫组化研究发现结节性多动脉炎患者炎症部位有大量的巨噬细胞和T淋巴细胞(主要为CD4 )浸润,这些T细胞表达大量的淋巴细胞活化标记,如IL-2、HLA-DR抗原等,提示T细胞介导的免疫机制在结节性多动脉炎的发病过程中起一定作用。
无论是细胞因子、抗内皮细胞抗体还是T细胞介导的免疫机制都不是结节性多动脉炎所特有的,也见于其他
系统性血管炎如韦格纳肉芽肿、Churg-Strauss综合征等。
2.病理
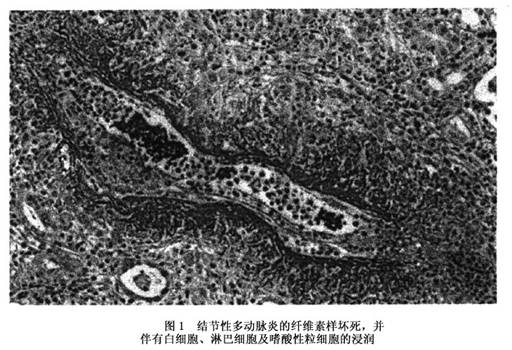
(1)结节性多动脉炎的病理一般表现为中、小肌动脉的局灶性的血管全层的坏死性炎性损伤。很少累及微小动脉和小静脉。病变好发于血管分叉处。机体的任何部位的动脉均可受累,但通常很少累及肺及脾脏动脉。急性期血管炎症损伤的特点主要表现为纤维素样坏死和多种细胞的浸润,浸润细胞主要为多形核白细胞、淋巴细胞及嗜酸性粒细胞。正常血管壁的结构被完全破坏(图1),同时可见有动脉瘤和
血栓形成。
(2)结节性多动脉炎病理改变的另一特点是同一患者活动性病变和已愈合的
血管损伤可同时存在(图2)。要确定不同器官的受累情况很困难,因为在很多的研究中病人的来源差异很大。在尸检病例报告中,结节性多动脉炎患者肾脏和心脏受累大约占70%,肝脏和胃肠道受累约占50%,外周神经受累也占50%,肠系膜受累占30%,骨骼肌受累占30%,中枢神经系统受累占10%,而皮肤受累发生率变异较大(从2%~50%)(图3,4)。
 临床表现
临床表现
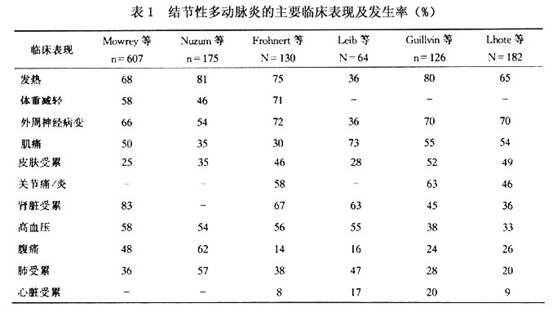
临床表现:结节性多动脉炎的临床表现多种多样。可急性或者隐匿性起病,疾病的严重程度因人而异,有的只表现为轻微的局限性病变,有的可表现为严重的全身多器官受累,并迅速恶化,甚至死亡。事实上,全身的任何器官可能最终都会受累,其发生率文献报道不完全一样,见表1。典型的全身性表现有发热,发热可呈持续性或间歇性,体温可高达39℃以上,也可为低热。另外还可有疲劳不适感,食欲不振,体重下降等表现。随着不同器官受损的出现可出现相应的临床表现。
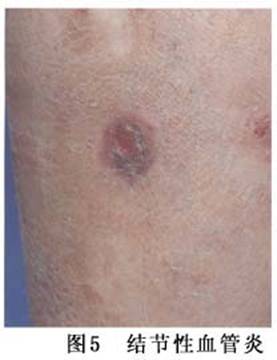
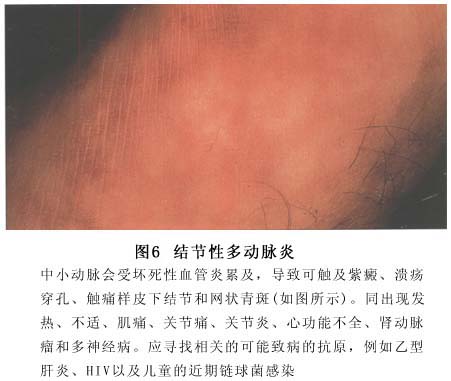
1.皮肤表现 25%~52%的多动脉炎患者有皮肤病变。皮肤受累的表现多种多样,最常见的表现是血管性紫癜。另外还可出现溃疡、网状青斑性血管炎、皮下结节及远端指(趾)缺血或坏死等。部分患者可有雷诺现象。皮肤活检主要为小血管和毛细血管的坏死性炎症。皮肤活检应包括真皮层才能测定是否有中等大小的血管受累。单靠皮肤活检不能确诊结节性多动脉炎,但结合其他的临床表现,皮肤活检对多动脉炎的诊断具有十分重要的意义(图5)。
2.关节和肌肉表现 有46%~63%的患者有关节炎或关节痛的表现。关节炎可出现在疾病的早期,也可伴随于整个疾病的过程中。有20%的患者可表现为下肢大关节的非对称性及非变形性的多关节炎,且大多出现在疾病的早期阶段。关节滑膜检查常无异常发现或仅有轻度白细胞浸润。骨骼肌中、小动脉受累,常表现为多发性肌痛和间歇性跛行(图6)。
3.神经系统表现 有36%~72%的结节性多动脉炎患者有神经系统受累。神经系统受累有时是患者最早期的临床表现。周围神经和中枢神经系统均可累及,但以前者多见。两者也可同时出现。受累的部位下肢比上肢更常见。症状可突然出现,表现为周围神经分布区的麻木和疼痛。约在数小时或数天后出现该部位运动和感觉障碍。随着疾病的进展,其他的外周神经也有受累而表现为多发性单神经炎(mononeuritis multiplex)。最终可出现累及所有感觉和运动神经的对称性多神经病(symmetric polyneuropathy)。少数患者可表现为进展缓慢的肢端感觉神经病变或脑神经
麻痹。约有10%~20%的结节性多动脉炎患者有中枢神经系统受累,临床表现包括
头痛、癫痫发作、脑神经功能异常、颅内出血和中风等。如果大脑、小脑或脑干动脉受累则表现相应部位的功能障碍,如
共济失调、舞蹈病等,但临床上较少见。
4.肾脏表现 临床上有45%~83%的结节性多动脉炎病人有不同程度的肾脏损害。主要表现为蛋白尿和红细胞管型尿。少数病人可呈
肾病综合征表现。血管性肾病是经典的结节性多动脉炎患者最常见的表现。结节性多动脉炎一般无肾小球肾炎的表现。肾血管的病变可导致肾的多发性梗死,最后可发展为肾功能衰竭。肾血管造影常显示有多发的动脉瘤和梗死灶。临床上可同时有高血压的表现,结节性多动脉炎的高血压通常较轻,有时是惟一的临床表现。
恶性高血压多见于那些
乙肝病毒感染的结节性多动脉炎患者。
5.胃肠道表现 胃肠道受累是结节性多动脉炎最严重的临床表现之一。
腹痛是胃肠道受累最常见和最早出现的临床症状,并且与病变的部位大致相关。另外还可表现为
腹泻、胃肠道出血和肝功能异常等。值得注意的是血管造影所见的病变部位及严重程度与胃肠道的临床表现及程度并无明显的相关。
肠缺血可表现为难治性
腹痛同时伴有体重下降。在大多数病例中,小肠缺血较常见。但结肠和胃的缺血很少发生。弥漫性
腹痛应考虑到肠系膜动脉栓塞的可能。如肠系膜动脉部分阻塞或其分支梗死,常表现为脂肪痢和体重下降,严重时有绞痛、血便及不完全性
肠梗阻表现。合并胃肠道溃疡时,可表现为嗳气、食欲不振等。并发溃疡穿孔时则表现为急腹症,严重者可导致死亡。上下消化道的血管炎还可引起呕血和黑便,但一般出血量不大。如果是动脉瘤破裂或坏死的动脉壁破裂,可引起大出血。
在尸检中肝脏病变较为常见,但临床上除常见有
乙肝病毒感染(HB抗原或抗体阳性)的证据外,无明显的临床症状。一般只见有转氨酶升高,提示可能有肝脏损害的存在。虽然可有肝血管的受累,但肝穿刺常无明显的异常发现。与
乙肝病毒感染相关的结节性多动脉炎患者的胃肠道表现比无
乙肝感染的患者要多见。胰腺受累时可表现为急性胰腺炎。阑尾和胆囊的血管炎较少见,但有时可能是结节性多动脉炎最初的临床表现。
临床上不能用结石或感染解释的胆囊炎及其他胃肠道症状应考虑结节性多动脉炎的可能。内窥镜检查及其活检对结节性多动脉炎胃肠道受累的诊断帮助并不很大,但可帮助鉴别非血管炎引起的
腹痛。严重的胃肠道症状提示预后不好。
6.心脏表现 虽然病理学检查心脏受累很常见,但临床表现却较少且易被忽视。冠状动脉炎可引起心绞痛、
心律失常,严重者则可发生心肌梗死、心力衰竭。心包炎罕见。20%的患者可出现心脏扩大。本病如出现胸痛,应警惕心绞痛或心肌梗死的可能。各种
心律失常均可出现,主要为室上性心动过速。心力衰竭也是本病的主要致死原因之一。
7.肺部表现 结节性多动脉炎的肺部表现包括肺部浸润、结节、空洞或间质纤维化。肺部浸润可呈弥漫性,常在其他器官受累之前出现。这种患者常常存在其他的基础病变如干燥综合征等。
8.其他表现 弥漫性的骨骼肌动脉受累可引起缺血性疼痛和间歇性跛行。30%~70%的患者有肌痛的症状,但广泛的肌病和肌酶谱升高并不多见。尸检发现80%的男性有附睾和睾丸受累,但临床症状如睾丸疼痛和硬结肿胀等并不多见。结节性多动脉炎出现眼部症状的约占10%,可表现为中心
视网膜动脉阻塞、
视盘水肿、脉络膜炎、虹膜炎、巩膜炎及结合膜出血等。颞动脉受累并不常见,常表现为咀嚼痛,病理结果示纤维素样坏死而无巨细胞浸润,这可与
巨细胞动脉炎相鉴别。
9.儿童表现 儿童的多动脉炎极为少见。主要有两种不同的类型:一是婴儿型,发生于2岁以内的婴儿,其临床表现与Kawasaki病相似,多脏器的受累少见,但常有不同类型心脏受累的表现。另一类型见于较大的儿童,其临床表现与成人相似。
10.特殊类型的结节性多动脉炎
(1)皮肤型多动脉炎:病变只局限在皮肤及皮下组织的动脉而无明显内脏受累的血管炎称为皮肤型多动脉炎(cutaneous polyarteritis),约占结节性多动脉炎病例的10%。皮肤型多动脉炎的组织病理与典型结节性多动脉炎无明显差别。在临床上主要表现为皮肤紫癜、疼痛性的皮下结节和网状青斑等。皮下结节一般为0.5~1.0cm大小,质地较硬,单个或多个,大多沿浅表动脉分布。结节中心可发生坏死形成溃疡,边缘不齐。皮损多见于下肢小腿,也可见于前臂、躯干、头面部及耳垂等部位。一般无全身症状,或可伴有低热、关节痛、肌痛等不适。病程与过敏性血管炎的表现相似,相对较长。大部分患者常呈自限性,预后良好。皮肤型多动脉炎对激素的治疗反应良好,但容易复发,可发展为系统性的结节性多动脉炎。
(2)继发性多动脉炎:许多疾病如类风湿关节炎、
系统性红斑狼疮、干燥综合征及少数毛细胞白血病等,可以合并多动脉炎。其血管炎的临床表现及病理改变与结节性多动脉炎相似。
 其他辅助检查
其他辅助检查
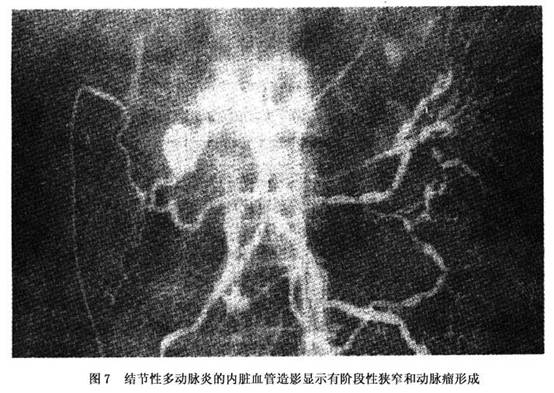
其他辅助检查:血管造影常发现有肾脏、肝脏、肠系膜及其他内脏器官的中等大小动脉有微小动脉瘤形成和节段性狭窄(图4)。微小动脉瘤形成虽不是结节性多动脉炎的特征性改变,但很常见。相反,动脉瘤很少见于抗中性粒细胞相关性血管炎(韦格纳肉芽肿病、Churg-Strauss综合征和显微镜下多血管炎)。在其他检查无异常发现时,血管造影是一有用的诊断工具。结节性多动脉炎的内脏血管造影显示有节段性狭窄和动脉瘤形成(图7)。
肾脏活组织检查 活检是最重要的诊断方法。取活检标本的部位可以是皮下结节和皮疹、有疼痛的肌肉或受累神经的邻近组织,亦可考虑睾丸和肾脏活检。活组织检查应包括弹性纤维染色,有助于见到破裂的弹力层。应尽量避免盲目的内脏活检,因为深部活检可能伤及动脉瘤,有造成大出血的危险。
肾脏活检组织病理所见如下:
1.肉眼观察 部分病例可见肾脏增大,多数病例肾脏仅见轻度改变或不规则的萎缩、梗死和斑点状出血,肾脏表面高低不平。动脉瘤破裂可引起肾内和肾周血肿,偶可见肾乳头坏死。
2.光镜检查 可见动脉、肾小球、肾小管、间质各部受累的病理改变。
(1)血管:主要累及弓形动脉,叶间动脉和小叶间动脉亦可受累。病变以肾皮质为主。肾多动脉炎伴肾梗死,纤维蛋白样坏死伴急性炎症,成纤维细胞增生,局部区域纤维化,血栓形成、管腔阻塞呈节段受累,主要涉及血管分叉处。动脉壁弹力层广泛节段性病变破裂成碎片是结节性多动脉炎的重要特征。肾血管病变具有特征性病理四期病损,发生率为70%~85%。
(2)肾小球:在结节性多动脉炎的急性坏死性血管炎中,肾小动脉、肾动脉的炎症和坏死性损害总是伴有肾小球病变。主要可见两种类型病理改变:肾小球缺血和细胞增生。各个小球病变程度及时期不一,有时在一个小球中有活动的和愈合的病灶同时存在。
肾小球缺血是由于血管壁狭窄或阻塞,
肾血流量减少所致,引起血管收缩缺血和肾小囊增宽被结缔组织所填满。
肾小球细胞增生,初时为局灶节段性,毛细血管内常有微血栓形成,纤维素样坏死,随后巨噬细胞浸润伴上皮反应形成大小不等的细胞新月体,呈弥漫性毛细血管外增生性肾小球肾炎,可同时伴弥漫性系膜和内皮细胞增生。小球病变亦可表现为单纯局灶、局灶硬化性肾小球肾炎,其占15%~20%。
免疫荧光存在部分
纤维蛋白原肾小球毛细血管壁沉着,很少有免疫球蛋白和补体在肾小球和小动脉壁沉积。
(3)肾小管:肾小管损害无特异性,由于肾动脉受累造成继发性缺血性损害,肾小管萎缩、坏死。临床可有相应的小管功能不足表现。
(4)肾间质:坏死性血管炎中,肾间质有不同程度的水肿,淋巴细胞、
浆细胞和多核细胞浸润,其中亦可有部分嗜酸性粒细胞,病变后期出现不同程度的间质纤维化。
 诊断
诊断
诊断:
1.结节性多动脉炎初发的临床表现各不相同,早期不易确诊。大多数患者有全身性表现如乏力、发热和体重下降等。如同时有皮肤损害,周围神经病以及肾脏病变等多系统受累则高度提示结节性多动脉炎的诊断。
风湿性多肌痛综合征或大关节受累的寡关节炎也可能是结节性多动脉炎早期的临床表现。提示结节性多动脉炎诊断的一些关键的临床表现为:
(1)全身性表现:发热,寒战,疲乏,体重下降,周身不适。
(2)关节痛或肌痛。
(3)多器官受累,包括。
①皮肤损害(紫癜,网状表斑,坏死性损伤,肢端坏死)。
②周围神经病变(多发性单神经炎)。
③尿沉渣异常,高血压。
虽然结节性多动脉炎的诊断主要根据临床表现,但活检和血管造影是确诊结节性多动脉炎的重要依据:①活检:如病理证实有中、小动脉的坏死性血管炎则提示本病的可能,但无特异性。活检的阳性率与取材部位有关。在有相应症状体征的器官和组织取材,阳性率相对较高。②血管造影:也无特异性,但可提示有无
系统性血管炎存在。
2.1990年美国风湿病协会提出了结节性多动脉炎的分类标准(表2)。1994年在美国Chapel Hill召开的国际血管炎会议又提出了结节性多动脉炎的定义标准,即:中、小动脉的坏死性炎症,无微动脉、毛细血管和小静脉受累,无肾小球肾炎。目前临床上主要参考这两个标准来诊断结节性多动脉炎。许多学者认为Chapel Hill会议制定的标准较狭窄,按这标准诊断,结节性多动脉炎的发病率非常低,因此它的临床实用性尚需进一步的研究。
3.1990年美国ACR关于PAN的分类(诊断)标准,符合下列标准中3条或3条以上者可确诊:
(1)体重下降≥4kg,除外节食或其他因素。
(2)网状青斑:四肢或躯干呈斑点及网状斑。
(3)睾丸疼痛或触痛:除外由于感染、外伤或其他原因所致。
(4)肌痛、无力或下肢触痛。弥漫肌痛(除外肩带肌和髋带肌)及肌无力或下肢肌触痛。
(5)单神经病或多神经病。
(6)舒张压≥12.0kPa(90mmHg)。
(7)肌酐、尿素氮升高:血肌酐≥132.7μmol/L(1.5mg/dl)或血尿素氮≥14.3mmol/L(40mg/dl)。
(8)乙型肝炎病毒:血清中检测到HBsAg或HbsAb。
(9)血管造影异常:包括内脏血管动脉瘤或阻塞,除外动脉硬化。
(10)中小动脉活检:病理示动脉壁内有粒细胞和(或)单核细胞浸润。
 鉴别诊断
鉴别诊断
鉴别诊断:
1.微型多发性动脉炎(MPA) 本病与乙型肝炎病毒无关。多累及小血管及小静脉、毛细血管。主要表现为肺
肾综合征,可出现肺
大咯血,肾小球肾炎(血尿、蛋白尿、
肾病综合征、急进性肾衰等表现),肾病理显示节段坏死性肾小球肾炎伴新月体形成,无免疫复合物沉着,免疫荧光阴性,血管造影无动脉瘤。P-ANCA,抗MPO抗体阳性率高。
2.大动脉炎 本病也可引起高血压,但血管造影显示主要累及主动脉及分支动脉,病理为肉芽肿病变,多发性单神经炎少见。
3.韦格纳肉芽肿 本病常累及小血管并形成肉芽肿,以鼻、鼻旁窦、肺、肾病变为主。胞浆型C-ANCA及抗蛋白酶3(PR3)抗体阳性率高,肾病理同MPA。
4.Chury-Strauss病 常有过敏性哮喘,外周血嗜酸性粒细胞>1.0×109/L,血清IgE升高。病变累及中、小动静脉。可见血管内及外肉芽肿。嗜酸性细胞组织浸润明显。
5.
系统性红斑狼疮 本病也有多系统损害。但免疫学检查常有C3下降,抗核抗体阳性,抗dsDNA阳性,抗Smith抗体阳性。肾病理示各型肾小球肾炎,肾小球毛细血管白金耳样改变,免疫荧光示IgG、IgA、IgM、C3共同沉积。
 治疗
治疗
治疗:本病在采用皮质激素治疗前,患者常出现暴发性死亡,多系统受累的患者大多于1年内死亡,5年生存率仅13%。自采用激素治疗后,5年生存率提高至48%~57%,10年存活率为42%。故目前激素仍为治疗本病的主药,激素的应用可有效控制本病的血管炎症。
1.肾上腺皮质激素 急性期重症可用甲泼尼龙冲击治疗,剂量为1g/d,加入生理盐水(NS)100ml中静脉滴注,滴注速度为60min以上,连续3天,然后改泼尼松(强的松)1mg/(kg•d),治疗6~8周,以后每1~2周减少原治疗量的10%,最后以10mg以下维持治疗,疗程6个月。对严重暴发性的患者,一般采用泼尼松(强的松)60~80mg/d,开始每天剂量分为每6小时1次,口服。待病情控制或稳定后,激素总量可逐步减少,最后以每天或隔天5~10mg,1次口服。神经系统受累及的患者,剂量可加大至80mg/d以上,并可加用细胞毒制剂治疗,两药联合应用对缓解本病有益,常用药物有环磷酰胺(CTX)、硫唑嘌呤、巯嘌呤等。
2.免疫抑制剂 以环磷酰胺(CTX)疗效最好。口服2mg/(kg•d),维持半年以上。如为重症可行冲击治疗,冲击量0.5~1.0g/次,间隔1~4周,维持间隔期不超过3个月。疗程一般1~2年。
3.非甾体类消炎药及秋水仙碱 用以治疗无内脏累及的皮肤型PAN。皮肤型PAN症状治疗大部分有效,如并有神经炎则要配合激素治疗。
4.
血浆置换(plasmapheresis) 在皮质激素和免疫抑制剂治疗无效的病例,可考虑
血浆置换,其有效率为41.7%。
5.乙型肝炎病毒相关结节性多动脉炎,可配合抗病毒药物如干扰素。
6.其他 对肾性高血压患者应积极降压治疗,临床常使用普萘洛尔和卡托普利(Captopril)、依那普利(Enalapril)等抑制肾素分泌和血管紧张素转换酶的降压药物,不但能有效降压,而且可以避免因高血压导致肾功能更趋恶化。
若患者已进入终末期肾功能衰竭,则应按常规进行透析,病情稳定后可作肾移植手术。
有血栓形成、血管闭塞、坏死者可采用抗凝药物,在肾动脉瘤破裂出血时可行血管内栓塞治疗而避免手术,导管栓塞无效可考虑外科手术治疗。有少数报告本病可使用大剂量人血丙种球蛋白治疗。
 预后
预后
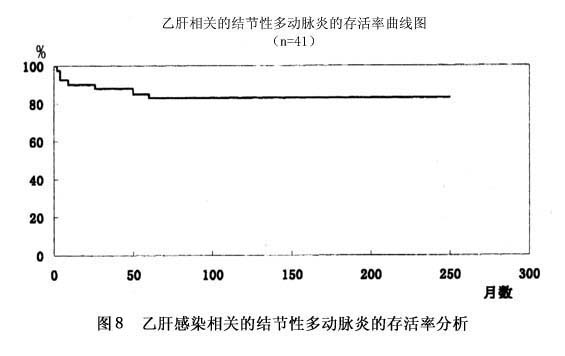
预后:结节性多动脉炎的预后取决于是否有内脏和中枢神经系统的受累及病变的严重程度。未经治疗的结节性多动脉炎的预后相当差,其5年生存率小于15%。单用激素治疗5年存活率为48%~57%。近年来由于激素及细胞毒药物的联合应用,生存率有明显的提高。大多数的研究表明5年生存率在50%~80%之间。Lhote F等报告41例有乙型肝炎感染的结节性多动脉炎患者用激素加抗病毒及血浆交换治疗后10年的存活率为83%(图8)。多数患者死亡发生于疾病的第1年。引起死亡最常见的原因是由于诊断不及时导致血管炎病变本身未能得到控制,另一个常见的原因是免疫抑制剂的使用引起的严重感染图8。
一般认为,如果患者的年龄在50岁以上,尿蛋白每天大于1g,肾功能不全,以及有心脏、胃肠道或中枢神经系统受累则病死率明显升高。但有外周神经系统受累如多发性单神经炎并不引起病死率的增加。
结节性多动脉炎的复发率比
显微镜下多血管炎的复发率要低,一般为10%。复发时的表现与最初的临床表现较为相似。



 流行病学
流行病学
 病因
病因
 发病机制
发病机制



 临床表现
临床表现
 并发症
并发症
 实验室检查
实验室检查
 其他辅助检查
其他辅助检查
 诊断
诊断

 鉴别诊断
鉴别诊断
 治疗
治疗
 预后
预后